Yeni Beyin Hücreleri Büyütülebilir mi? Yeni Araştırma Bu Süregelen Bilimsel Tartışmaya Kesin Cevap Sunuyor
On yıllardır, insan beyninin erken çocukluk döneminden sonra büyük ölçüde durağanlaştığı ve milyarlarca nöronun değişmeden kaldığı, yaşla birlikte azalacağına inanılıyordu. Bu kavrayış—bilimsel literatürde ve popüler inançta bir temel taşı olarak—bir kez beyin hücreleri (nöronlar) öldüğünde, sonsuza dek yok oldukları iddia ediliyordu. Ancak, son bilimsel ilerlemeler bu bakış açısını alt üst etti. Sinirbilim, moleküler biyoloji ve rejeneratif tıptaki atılımlar, yetişkinlikte bile yeni beyin hücreleri geliştirmenin potansiyelini, yani nörogenezi ortaya çıkardı. Bu makale, bu tartışmanın tarihsel gelişimini, hücre büyümesinin biyolojisini, beyin hücresi yenilenmesi konusundaki son araştırmaları ve hücre büyümesi tekniklerinin gelecekteki uygulamalarını keşfederek, mevcut bilimsel oybirliği ile sonuçlanıyor.
Önemli noktaları göster
- Bir zamanlar beyin hücrelerinin çocukluktan sonra yenilenmediğine inanılıyordu, ancak son keşifler bunun aksini kanıtlıyor.
- Nörogenez hakkındaki anlayış 19. yüzyılın sonlarında hücre teorisi önerileriyle başladı.
- Bu alandaki araştırmaları geliştirmek için gen düzenleme ve görüntüleme teknolojileri gibi ileri teknikler geliştirildi.
-
- Epitelyal, kan, kalp, karaciğer ve sinir kök hücreleri gibi çeşitli hücre türleri kültürlenebilir.
- Pankreas beta hücreleri, retinal hücreler ve kortikal nöronlar gibi bazı hücrelerin kültürlenmesinde zorluklarla karşılaşılmaktadır.
- Kültürlenmiş hücreler deri grefti, kanser tedavisi ve nörolojik rehabilitasyonda kullanılır.
- Son çalışmalar çevresel ve sağlık faktörleriyle etkilenerek yaşam boyu hipokampal nörogenezi doğrulamaktadır.
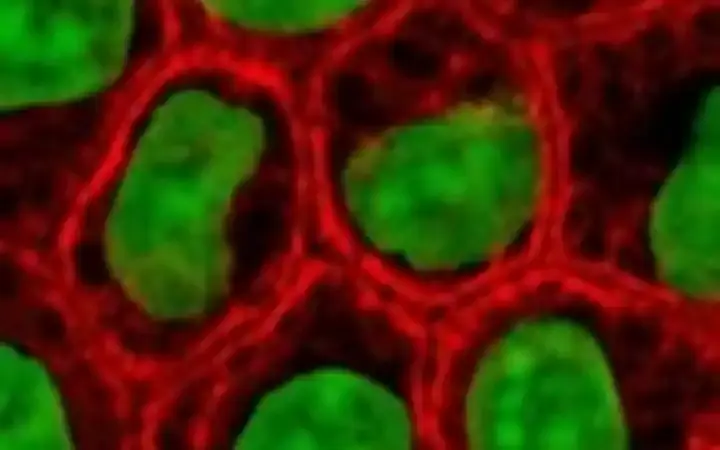
Kültürdeki epitelyal hücreler, keratin (kırmızı) ve DNA (yeşil) ile boyanmış
1. Hücre Büyümesinin Tarihi ve Gelişimi.
Hücre büyümesini anlama yolculuğu 19. yüzyılın sonları ve 20. yüzyılın başlarında, özellikle Theodor Schwann'ın 1839’da hücre teorisini ilan etmesi ve Santiago Ramón y Cajal'ın sinirbilimde öncülük eden çalışmaları sonrasında başladı. Cajal ünlü bir şekilde şu ifadeyi söyledi: "Yetişkin beyinlerde sinir yolları sabittir, sona ermiştir ve değişmezdir. Her şey ölebilir, hiçbir şey yeniden doğamaz."
Bir büyüme ortamında büyüyen kültürlü hücreler
1960'lara kadar Amerikalı sinirbilimci Joseph Altman bu inancı meydan okuyarak yetişkin sıçanların beyinlerinde yeni nöronlar tanımladı (Altman ve Das, 1965). Bulguları hakim inanışlar ve sınırlı görüntüleme teknikleri nedeniyle geniş ölçüde reddedildi. Konsept, bilim insanlarının yeni hücre doğumlarını izlemelerine olanak tanıyan BrdU (bromodeoksiüridin) gibi konfokal mikroskoplar ve hücre etiketleme tekniklerinin geliştirilmesiyle 1990'larda yeniden gündeme geldi.
2. Hücre Büyümesindeki Anlayışın Evrimi.
Hücre yenilenmesini anlamak, kök hücre devrimi ile önemli ölçüde genişledi. İlk olarak 1981'de farelerde ve 1998'de insanlarda izole edilen kök hücreler—özelleşmiş hücre türlerine farklılaşabilen—kalp, karaciğer ve deri hücreleri de dahil olmak üzere hasarlı dokuları yenilemenin yolunu açtı.
2000'lerin başlarına gelindiğinde, araştırmacıların belirli beyin bölgelerinde sinir kök hücrelerini (NSC'ler) tanımlamaya başladığı sinir sistemine dikkat çekildi. Hipokampus ve subventriküler alan, yetişkin nörogenez için anahtar bölgeler olarak ortaya çıktı.
Ekonomik Görünüm: Küresel kök hücre tedavisi pazarı, 2030 yılına kadar 30,1 milyar ABD Dolarına ulaşması bekleniyor, nörolojik rejeneratif terapiler önemli bir kısmını oluşturacak.

DMEM hücre kültürü ortamı şişesi
3. Hücre Kültürlemekteki Son İlerlemeler.
Teknolojik keşifler, hücrelerin kültürlenme ve kontrol edilme yeteneğini önemli ölçüde geliştirdi:
• Organoidler: Kök hücrelerden büyütülen küçük beyin yapıları beyin büyümesini taklit eder ve nörogenez araştırmaları için yeni bir model sunar.
• CRISPR-Cas9 ile gen düzenleme, hücre büyümesini ve onarımını düzenleyen genlerin mikro yönetimini mümkün kıldı.
• Tek hücreli RNA dizileme, hücre türlerini sınıflandırmak ve gelişimsel soylarını izlemek için yardımcı oldu.
2019'da, Boldrini et al. (Columbia Üniversitesi) tarafından yapılan bir dönüm noktası çalışması, yaşlılarda devam eden hipokampal nörogenez delilleri sundu, yaşa bağlı hafıza gerilemesinin kaçınılmaz olmadığını öne sürdü.
4. Kültürlenebilecek Hücre Türleri ve Kategorileri.
Kültürü yapılabilir Hücreler:
• Epitelyal Hücreler: Deri ve kaplama dokuları, laboratuvarda kolayca kültürlenebilir.
• Hematopoetik Hücreler: Kemik iliği kök hücrelerinden türetilen kan hücreleri.
• Hepatik Hücreler: Karaciğer yeniden doğuşu dokümante edilmiş bir doğal fenomendir.
• Kardiyak Hücreler: Son zamanlarda kalp krizi sonrası kök hücre tedavisi ile yeniden doğduğu gösterilmiştir.
• Sinir Kök Hücreleri: Nöronlara, astrositlere ve oligodendrositlere farklılaşabilme yeteneğine sahiptir.
İstatistiksel Bilgi: Ulusal Sağlık Enstitüleri'ne göre, 80’den fazla klinik deneme şu anda Parkinson hastalığı, inme iyileşmesi ve omurilik zedelenmelerini tedavi etmek için kültüre edilmiş sinir kök hücrelerini kullanmaktadır.
5. Büyümesi Zor Hücreler.
Bazı hücreler yenilenmeye veya yapay olarak kültürlenmeye dirençli kalmaktadır:
• Pankreatik Beta Hücreleri (insülin üreten): Vücut dışında güvenilir bir şekilde çoğalması zordur.
• Retinal Hücreler: İlerlemiş olmasına rağmen, tam görüş restorasyonu hala karmaşıktır.
• Olgun Kortikal Nöronlar: Tam olarak olgunlaştıklarında, sinir ortamları dışında yenilenmeleri daha az olasıdır.
Ek olarak, bağışıklık reddi, mutasyon riski ve destekleyici iskelet sınırlamaları, belirli özel hücre türlerinin büyümesini zorlaştırmaktadır.
6. Hücre Kültürlemenin İleri Uygulamaları.
Kültürlenmiş veya yeniden doğmuş hücreler şu anda şu alanlarda kullanılmaktadır:
• Yanık kurbanları için deri greftleri.
• Lösemi hastaları için kemik iliği nakilleri.
• Miyokard enfarktüsü sonrası kalp onarımı.
• Nörolojik rehabilitasyon (Parkinson ve omurilik zedelenmeleri gibi).
• Laboratuvarda geliştirilen organoidler kullanılarak ilaç testi.
Ekonomik Veriler: Rejeneratif tıp pazarı, 2035 yılına kadar dünya çapında 150 milyar ABD Dolarını aşması bekleniyor.
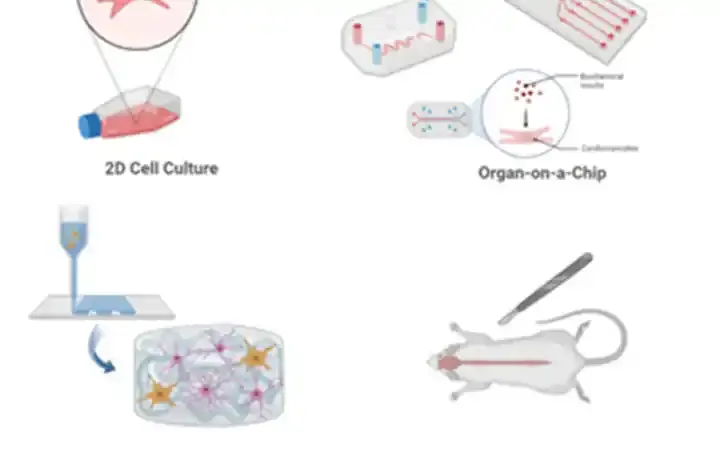
2D kültürü, 3D yetiştirme, organ-on-chip çalışması ve in vivo çalışmanın diyagramı
7. Beyin Hücreleri Kültüre Edilebilir mi?
Evet, ancak bazı koşullarla. Nörogenez, şu beyin alanlarında doğrulanmıştır:
• Hipokampal Dişli Girus: Öğrenme ve hafıza ile bağlantılıdır.
• Subventriküler Bölge: Koku soğancığına nöronlar sağlar (özellikle kemirgenlerde).
Ancak, kortikal nöronların geniş çaplı yenilenmesi henüz kılavuzdan yoksundur. Yine de, indüklenmiş pluripotent kök hücrelerden (iPSCs) ve beyin organoidlerinden laboratuvarda yetiştirilen beyin hücreleri, sinir davranışlarını kısmen taklit etmede başarı göstermektedir.

Nörogenez, yani yeni nöronların oluşumu doğum öncesi meydana gelir, ancak bazı kanıtlar yaşam boyu devam edebileceğini öne sürmektedir
8. Beyin Hücresi Büyüme Tartışması.
Biriken kanıtlara rağmen, bu alan yoğun bir tartışma ile karşı karşıya :
• Savunucular: Eriksson et al. (1998) ve Boldrini et al. (2018) gibi çalışmaları yaşam boyu hipokampal nörogenezi desteklediğini belirtmektedir.
• Şüpheciler: Sorrells et al. (2018) gibi çocukluk sonrası nörogenezde keskin bir düşüş yaşandığı iddialarını ileri sürmektedir.
Bu tartışma, metodolojik farklılıklardan, doku korunma kalitesinden ve görüntüleme duyarlılığından kaynaklanmaktadır.
9. Beyin Hücresi Büyümesi Üzerine Yeni Araştırma ve Son Cevap.
2023 yılında, Allen Beyin Bilimleri Enstitüsü ve Stanford Üniversitesi tarafından yapılan bir dönüm noktası meta-analiz, 40'tan fazla çalışmayı inceleyerek şöyle bir sonuca vardı: "Yetişkin hipokampal nörogenez memelilerde, insanlar da dahil olmak üzere korunmuş ve devam eden bir süreç olup, yaş, çevre ve sağlık tarafından belirlenen çeşitlilikler göstermektedir."
Ayrıca, fiziksel egzersiz, zenginleştirilmiş çevreler ve diyet unsurları (örneğin, yaban mersininde bulunan flavonoidler) gibi nörogenezi artıran faktörler belirlenmiştir.
Dolayısıyla, nihai bilimsel uzlaşı, beyin hücrelerinin—özellikle hipokampusta—uygun koşullarda yaşam boyu boyunca büyüyebileceğini doğrulamaktadır.
10. Hücre Büyümesinin Geleceği ve Uygulamaları.
Hücre büyümesinin geleceği, sinirbilim, yapay zeka ve doku mühendisliği kesişiminde yatmaktadır:
• Alzheimer hastalarına hafızayı yeniden kazandırmak için biyomühendislik ürünü beyin implantları.
• Kişiselleştirilmiş nörolojik araştırmalar için genetik olarak modifiye edilmiş beyin organoidleri.
• Omurilik yaralanmalarını ve nörodejenerasyonu ele almak için nöron baskısı ve transplantasyonu.
• Gerçek biyolojik nöronlardan oluşturulmuş AI eğitilmiş sinir ağları (örneğin, DishBrain, 2022).
Tahmin: 2040 yılına kadar, nöronal rejenerasyon, şu anda yıllık 1 trilyon ABD Dolarından fazla maliyeti olan nörodejeneratif hastalıkların küresel yükünü %25'e kadar azaltabilir, bu WHO tahminlerine göre.
Sonuç,
İnsanların yeni beyin hücreleri büyütebilme sorusu, şüpheci bir efsaneden belgelenmiş bilimsel bir gerçeklik haline geldi. Moleküler biyoloji, kök hücre araştırmaları ve görüntüleme teknolojilerindeki ilerlemeler sayesinde, şimdi yetişkin nörogenezinin hipokampusta özellikle meydana geldiğini ve beyin yaralanmaları ve dejeneratif hastalıkların tedavisi için büyük potansiyel sunduğunu anlıyoruz. Tüm nöron türlerinin yeniden doğuşu konusunda zorluklar devam etse de, alan hızlı bir şekilde kesin beyin onarımına doğru ilerlemektedir. Bilim biyoloji ve mühendislik arasındaki sınırları bulanıklaştırmaya devam ettikçe, beyin hücrelerini büyütme yeteneği yakın gelecekte sadece terapötik bir olasılık değil, bilişi artırmanın temel bir yolu haline gelebilir.